Det er virkelig svært at få lægemiddelstoffer ind i hjernen og behandle sygdomme.
Hjernen har nemlig proteiner, der aktivt kan pumpe stoffer ud af blodkarrenes vægge igen. Man kan sige, at hvis hjernen er en eksklusiv klub, er pumpe-proteinerne en slags udsmidere, der står foran indgangen.
For at finde ud af om et nyt lægemiddelstof kan komme ind i hjernen, er det nødvendigt at undersøge lægemiddelstoffernes molekylære egenskaber for at se, om de er små og fedtede nok til trænge gennem blodkarrenes vægge.
I denne artikel vil jeg fortælle om, hvordan vi i min forskningsgruppe på Københavns Universitet arbejder med, hvordan vi kan snige gavnlige lægemidler igennem blodkarrene – udenom de barske udsmidere.
Store udfordringer med hjernesygdomme
Vi har oplevet en voldsom stigning i antallet af diagnosticerede hjernesygdomme i løbet af de sidste 10-20 år. Det gælder sygdomme som Alzheimers, Parkinsons, depression og en række andre sygdomme (se f.eks. her, her, her og her)
Noget af det skyldes formentlig, at vi bliver ældre. Noget andet er, at vi er blevet bedre til opdage og diagnosticere hjernesygdommene.
Desværre er det ikke lykkedes os, der arbejder med udvikling af ny medicin til hjernen, at følge med denne udvikling. Der er derfor rigtig mange mennesker, der har lidelser i hjernen, som vi ikke kan behandle med medicin.
Det skyldes to ting:
- For det første er der mange sygdomme i hjernen, vi endnu ikke forstår, og derfor ved vi ikke, hvordan vi skal fremstille medicin, der kan behandle dem.
- For det andet er det virkelig svært at få lægemiddelstoffer frem til hjernevævet.
I min forskningsgruppe arbejder vi med, hvordan vi kan få det aktive stof i lægemidler frem til de steder i hjernen, hvor de skal skabe en forskel (for at læse mere om det aktive stof i lægemidler, se boksen 'lægemidler versus lægemiddelstoffer' under artiklen).
Vi prøver at skabe kunstige hjernevæv i laboratoriet, særligt de dele af hjernevævet, der er med til at holde medicin ude af hjernen.
LÆS OGSÅ: Museforsøg: Hjernens små 'eksplosioner' kan stoppes, og det åbner for ny behandling mod epilepsi
Kun de små, fedtede stoffer bliver lukket ind
Det sted, hvor medicin holdes ude af hjernen, kaldes blod-hjerne-barrieren, og den udgøres af væggene i hjernens blodkar. For at komme fra blodet og ind i hjernen skal lægemiddelstoffer altså trænge gennem blodkarrernes vægge.
Det lyder måske enkelt nok, men væggene i hjernens blodkar skal beskytte hjernen mod uønsket påvirkning. Derfor er de enormt tætte, og kun meget små stoffer kan trænge mellem cellerne, der danner væggene i blodkarrene.
Stoffer, der er fedtede (lipofile), kan opløses i andre fedtstoffer. Den egenskab gør dem i stand til at gå igennem celler, fordi cellernes membraner netop er lavet af fedtstoffer (se mere i boksen 'fedtelskende stoffer' under artiklen).
Et fedtet stof kan altså bevæge sig fra blodet og ind i en cellemembran, videre gennem cellen og ud gennem cellemembranen på den anden side.
Denne proces kalder vi transcellulær diffusion, fordi stoffet passerer (altså diffunderer) tværs igennem cellerne.
Jagten på stoffer, der kan gå fra blodet til hjernen
Igennem de sidste mange år har forskere, der arbejder med medicin, sammenlignet de molekylære egenskaber af lægemiddelstoffer, der kan passere gennem biologiske barrierer ved at diffundere gennem cellemembraner.
Det har vist sig, at der er nogen fællestræk for de lægemiddelstoffer, der kan diffundere fra blod til hjerne:
- Molekylvægten skal være mindre end 400 Dalton (dvs. det skal være meget småt!)
- Molekylet skal være fedtet, men ikke alt for fedtet
- Molekylet må ikke have særligt mange grupper, der kan danne brintbindinger.
Dette sæt af regler kan bruges, når man designer lægemiddelstoffer til at lave molekyler, der vil have en god chance for at diffundere gennem blodkarrenes vægge.
Overholder man reglerne, har man altså en god chance, men ingen garanti. Man kan nemlig ikke forudsige om de nye, designede molekyler vil blive genkendt af hjernens udsmiderproteiner og holdt aktivt ude af hjernevævet – det skal derfor også undersøges.
LÆS OGSÅ: Nyt studie antyder: Vi får nye hjerneceller hele livet, men Alzheimer-patienter danner knap så mange
Efflux-pumperne skubber medicinen ud
Igennem de mange millioner af år hvor pattedyrhjernen er blevet udviklet, har vi fået bygget stærke forsvarsmekanismer til at holde uønskede stoffer ude. Hjernens efflux-pumper - dem vi hidtil har kaldt udsmiderproteinerne - er et eksempel på dette.
Efflux-pumper er membranproteiner, der sidder i karvæggenes yderste membran – den side, der sidder ud mod blodet. Her opfanger de en hel række af stoffer, der trænger ind i cellerne, og smider dem ud igen.
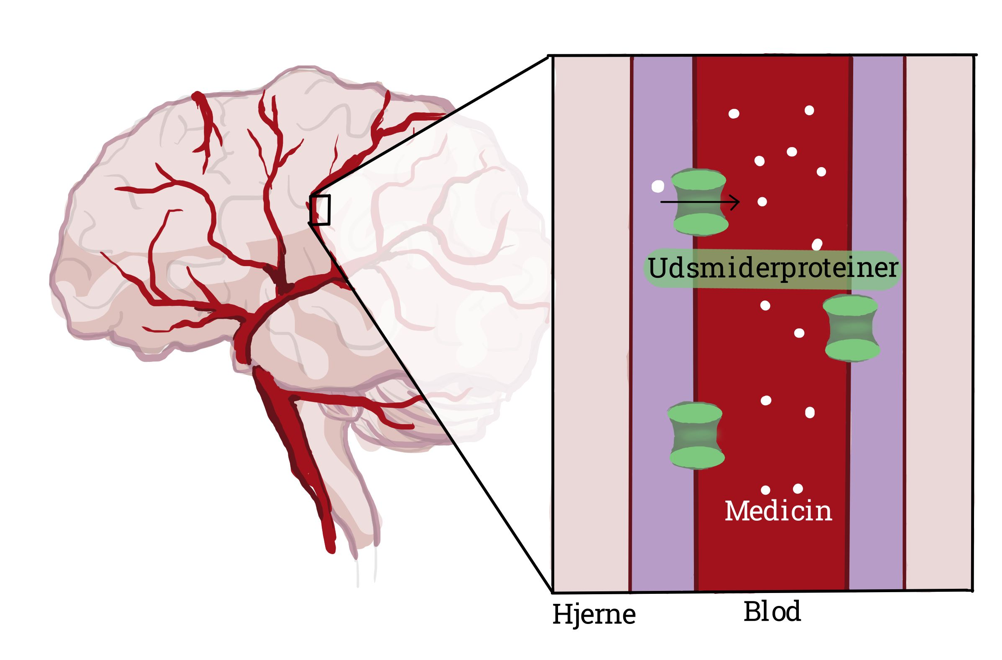
Som nævnt kan vi ikke vide os sikre på, om et nyt lægemiddel bliver lukket igennem hjernens vægge eller ej. Derfor skal vi for hvert eneste nye lægemiddelstof, vi laver, undersøge, om det bliver genkendt af pumperne.
Man kunne jo så lave en masse dyreforsøg, sprøjte det nye stof ind i blodet på mus, og se om stoffet når hjernen, eller om det bliver holdt ude af pumperne.
Men dels vil vi gerne holde brugen af forsøgsdyr på et så lavt niveau som muligt, dels er mus og mennesker forskellige på nogen områder – eksempelvis er pumpeproteinerne lidt forskellige i deres opbygning.
Vi kan altså ikke helt stole på, at de resultater, vi får i forsøg med mus, også vil gælde for mennesker. Så hvad gør vi så?
LÆS OGSÅ: Lægemidler skabes ved at finde 'molekylet i høstakken
Modeller i stedet for mus
Når vi nu hverken kan lave forsøg på mennesker (det gør man først sent i processen) eller stole helt på de resultater, vi har fra mus, laver vi cellemodeller med de menneskelige udsmiderproteiner.
Cellemodeller er enkeltlag af celler hvor vi har sat menneskelige udsmiderproteiner ind ved hjælp af genteknologi. Vi kan så dyrke cellerne i laboratoriet og måle, om udsmiderproteinerne fanger de nye lægemiddelstoffer, vi vil bruge til behandling (læs mere om cellemodellen her).
Trænger de fra blodsiden gennem cellelaget og ind til hjernesiden, er de velegnede. Trænger de ikke gennem cellelaget, men bliver holdt tilbage af pumperne, er de ikke velegnede til at komme ind i hjernen.
Stoffer, der viser sig som lovende kandidater i celleforsøg, bliver så derefter testet videre – først på dyr og siden på mennesker - mens de mange kandidater, der ikke klarer testen, bliver sorteret fra, og vi sparer en masse tid og forsøgsdyr.
LÆS OGSÅ: Alzheimer-hjerner indeholder større mængder herpesvirus
\ Forskerzonen
Denne artikel er en del af Forskerzonen, som er stedet, hvor forskerne selv kommer direkte til orde.
Her skriver de om deres forskning og forskningsfelt, bringer relevant viden ind i den offentlige debat og formidler til et bredt publikum.
Forskerzonen er støttet af Lundbeckfonden.
Stor interesse i at få endnu større stoffer forbi udsmiderne
Inden for vores felt har cellemodellerne gjort det muligt med relativt god nøjagtighed at forudsige, om hjernen vil optage lægemiddelstoffer inden for den stofklasse, der kaldes 'små molekyler', dvs. de meget små molekyler under 400 Dalton, som jeg nævnte tidligere.
Der er imidlertid en voldsom interesse i at få større molekyler ind i hjernen også, særligt terapeutiske antistoffer, der kan bindes til receptorer på hjerneendothelcellernes overflade.
Vi arbejder derfor også med at udvikle nye cellemodeller ud fra humane stamceller, hvor vi kan undersøge antistof-transport ved hjælp af receptorer.
Det er vores håb, at vores arbejde med modeller af menneskets blod-hjerne-barriere vil føre til en hurtigere udvikling af ny medicin og sætte os i stand til at bekæmpe den store stigning i antallet af diagnosticerede sygdomme i hjernen.
LÆS OGSÅ: Ny teori: Sådan vil forsker reducere alvorsgraden af migræne
LÆS OGSÅ: Når hjernerystelsen vender arbejdslivet på hovedet
\ Kilder
- Birger Brodins profil (KU)
- "Global, regional, and national burden of Alzheimer's disease and other dementias, 1990–2016: a systematic analysis for the Global Burden of Disease Study 2016", The Lancet (2019). DOI: 10.1016/S1474-4422(18)30403-4
- "Global, regional, and national burden of Parkinson's disease, 1990–2016: a systematic analysis for the Global Burden of Disease Study 2016", The Lancet (2018). DOI: 10.1016/S1474-4422(18)30295-3
- "Trends in depression prevalence in the USA from 2005 to 2015: widening disparities in vulnerable groups", Psychological Medicine (2018). DOI: DOI: 10.1017/S0033291717002781
- "Depression and Other Common Mental Disorders. Global Health Estimates", World Health Organisation (2017).
- "IPEC-J2 MDR1, a Novel High-Resistance Cell Line with Functional Expression of Human P-glycoprotein (ABCB1) for Drug Screening Studies", Molecular Pharmaceutics (2015). DOI: 10.1021/acs.molpharmaceut.5b00874
\ Lægemidler versus lægemiddelstoffer
Et lægemiddelstof er det aktive stof i et lægemiddel, der virker på den sygdomstilstand, man vil behandle.
Et eksempel er lægemiddelstoffet Paracetamol, der findes i forskellige tabletter mod hovedpine og smerter, som Panodil, Pamol m.fl.
Lægemidlet er hele den tablet, man indtager. En Panodil-tablet vil også indeholde stoffer, der får tabletten til at hænge sammen under produktion, stoffer der indgår i et overtræk, der gør, at man ikke kan smage den bitre smag som Paracetamol har, og stoffer som får tabletten til at smuldre hurtigt, når den kommer ned i mavevæsken.
Disse stoffer kaldes under et for hjælpestoffer, fordi de ’hjælper’ det aktive lægemiddelstof frem mod målet.
Hvis man er interesseret i at finde ud af, hvilke stoffer der er i et lægemiddel, kan man kigge i den såkaldte indlægsseddel, der følger med lægemidler fra apoteket.
\ Fedtelskende stoffer
Normalt vil man ikke skrive i en videnskabelig tekst, at et stof er fedtet, men at det er lipofilt (græsk ord, der betyder 'fedt-elsker').
Et stofs lipofilicitet (hvor fedt-elskende det er) kan bestemmes ved simple eksperimenter med vand og organiske opløsningsmidler.
Man tager simpelthen lige dele vand og organisk opløsningsmiddel (der kan betragtes som en slags tyndtflydende fedt) og hælder sammen. Og så hælder man sit lægemiddelstof i blandingen.
Vand og organisk lægemiddelstof vil ikke blandes, men skille i to faser, en vand- og en 'fedt'-fase.
Man måler så, hvor stor koncentrationen af stoffet er i hver af faserne. Dette forhold kaldes også fordelingskoefficienten og navngives P (efter det engelske Partition coefficient). Skrevet op på en formel måde får man en ligning, der siger:
P = [koncentration i organisk fase] / [koncentration i vandfase]
Man kan se af ligningen, at jo højere koncentrationen i fedtfasen er i forhold til vandfasen, jo højere vil P blive, og jo mere lipofilt er stoffet.