Liv og død bliver normalt betragtet som modsætninger, men nye flercellede livsformer fra cellerne i en død organisme introducerer en 'tredje tilstand', der falder uden for de traditionelle grænser for liv og død.
Normalt betragter forskerne døden som det uigenkaldelige ophør af en organismes funktioner. Men som eksempelvis organdonationer viser, kan organer, væv og celler fortsætte med at arbejde, selv efter en organismes død.
Denne evne rejser spørgsmålet: Hvilke mekanismer gør det muligt for bestemte celler fortsat at fungere, efter at organismen er død?
Vi er forskere, der undersøger, hvad der sker i organismer, efter de dør. I vores nyligt offentliggjorte gennemgang beskriver vi, hvordan visse celler har kapaciteten til at transformere til flercellede organismer med nye funktioner efter døden, hvis de bliver forsynet med næringsstoffer, ilt, bioelektromagnetisme eller biokemiske signaler.
Liv, død og noget helt nyt
Denne tredje tilstand udfordrer, hvordan forskere typisk forstår celleadfærd.
Larver, der metamorfoserer til sommerfugle, eller haletudser, der udvikler sig til frøer, er velkendte udviklingstransformationer, men der er kun få tilfælde, hvor organismer ændrer sig på måder, der ikke er forudbestemt.
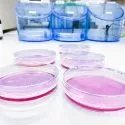
Tumorer, organoider og cellelinjer, der kan dele sig uendeligt i en petriskål, som for eksempel HeLa-celler, betragtes ikke som en del af denne tredje tilstand, fordi de ikke udvikler nye funktioner.
Forskere har fundet, at hudceller ekstraheret fra afdøde frøembryoner var i stand til at tilpasse sig de nye forhold i en petriskål i et laboratorium og spontant omorganisere sig til flercellede organismer kaldet xenobotter.
Disse organismer udviste adfærd, der strækker sig langt ud over deres oprindelige biologiske rolle.
Specifikt bruger disse xenobotter deres cilier - som er små fimrehår - til at navigere og bevæge sig i deres omgivelser, hvorimod cilierne i et levende frøembryo typisk bruges til bevæge slimlag.
Xenobots er også i stand til at udføre 'kinematisk selvreplikation', hvilket betyder, at de fysisk kan replikere deres struktur og funktion uden at vokse. Det adskiller sig fra mere almindelige replikationsprocesser, der involverer vækst i eller på organismens krop.
Forskerne har også fundet, at isolerede menneskelige lungeceller selv kan samle sig til multicellulære miniatureorganismer, der kan bevæge sig rundt.
Disse såkaldte 'anthrobotter' opfører sig og er struktureret på en ny måde. De er ikke kun i stand til at navigere i deres omgivelser, men reparerer også både sig selv og beskadigede nærliggende neuronceller.
Samlet set demonstrerer disse fund de cellulære systemers iboende plasticitet og udfordrer teorien om, at celler og organismer kun kan udvikle sig på forudbestemte måder. Den tredje tilstand peger på, at organismedød kan spille en væsentlig rolle i, hvordan livet transformerer sig over tid.
Post mortem-betingelser
Flere faktorer har indflydelse på, om visse celler og væv kan overleve og fungere, efter at en organisme dør, blandt andet miljøforhold, metabolisk aktivitet og præserveringsteknikker.
Forskellige celletyper har forskellige overlevelsestider.
For eksempel dør hvide blodlegemer hos mennesker mellem 60 og 86 timer efter organismens død. Hos mus kan skeletmuskelceller dyrkes igen efter 14 dage efter døden, mens fibroblastceller fra får og geder kan dyrkes op til omkring en måned post mortem.

Metabolisk aktivitet spiller en vigtig rolle for, om celler kan fortsætte med at overleve og fungere. Aktive celler, der kræver en kontinuerlig og stor tilførsel af energi for at opretholde deres funktion, er sværere at dyrke end celler med et lavere energibehov.
Præserveringsteknikker som kryopræservering kan gøre vævsprøver som for eksempel knoglemarv i stand til at fungere på samme måde som levende donorkilder.
Iboende overlevelsesmekanismer spiller også en nøglerolle for, om celler og væv lever videre.
For eksempel har forskere observeret en signifikant stigning i aktiviteten af stress-relaterede gener og immun-relaterede gener efter organismers død, hvilket sandsynligvis vil kompensere for tabet af homøostase (opretholdelse af indre ligevægt eller balance i for eksempel et biologisk system som kroppen).
Desuden påvirker faktorer som traumer, infektion og den tid, der er gået siden døden, vævets og cellernes levedygtighed markant.
Faktorer som alder, helbred, køn og art former yderligere post mortem-landskabet. Det ses i udfordringen med at dyrke og transplantere metabolisk aktive ø-celler, som producerer insulin i bugspytkirtlen (de såkaldte Langerhans' øer), fra donorer til modtagere.
Forskerne mener, at autoimmune processer, høje energimæssige omkostninger og nedbrydningen af beskyttelsesmekanismer kan være årsagen til, at det går galt i forbindelse med ø-celle-transplantationer.
Stort potentiale
Hvordan samspillet mellem disse variabler gør visse celler i stand til at fungere, efter at en organisme dør, er stadig ikke klart. En hypotese er, at specialiserede kanaler og pumper indlejret i de ydre membraner af cellerne tjener som komplicerede elektriske kredsløb.
Disse kanaler og pumper genererer elektriske signaler, der gør cellerne i stand til at kommunikere med hinanden og udføre specifikke funktioner som vækst og bevægelse, der former strukturen af den organisme, de danner.
Det er også usikkert, i hvilket omfang forskellige typer celler kan undergå transformation efter døden.
Tidligere forskning har fundet, at specifikke gener involveret i stress, immunitet og epigenetisk regulering (kontrol og regulering af vores arvemateriale, red.) aktiveres efter døden hos mus, zebrafisk og mennesker, hvilket peger på stort potentiale for transformation blandt forskellige celletyper.
Implikationer for biologi og medicin
Den tredje tilstand giver ikke kun ny indsigt i cellers tilpasningsevne, men også håb for nye behandlinger.
For eksempel kan 'anthrobotter' hentes fra et individs levende væv for at levere lægemidler uden at udløse en uønsket immunrespons. Konstruerede 'anthrobotter' indsprøjtet i kroppen kan potentielt opløse plak i årerne hos patienter med åreforkalkning og fjerne overflødig slim hos patienter med cystisk fibrose.
Det er vigtigt, at disse flercellede organismer har en begrænset levetid, som naturligt bliver nedbrudt efter fire til seks uger, for det forhindrer væksten af potentielt invasive celler.
En bedre forståelse af, hvordan visse celler fortsætter med at fungere og omdannes til flercellede enheder i et stykke tid efter en organismes død, kan potentielt hjælpe den videre udvikling af personlig medicin (også kaldt præcisionsmedicin) samt forebyggende medicin.
Denne artikel er oprindeligt publiceret hos The Conversation og er oversat af Stephanie Lammers-Clark.
\ Kilder
Læs om brug og viderebringelse af Videnskab.dk's artikler.